CYRAMZA LÀ GÌ
Là thuốc dạng dịch tiêm, chứa thành phần ramucirumab, là một kháng thể đơn dòng IgG1 tái tổ hợp có tác dụng kháng VEGFR2, do Eli Lilly phát triển và thương mại hóa. Cyramza được chỉ định điều trị bệnh nhân ung thư biểu mô tế bào gan (HCC) có alpha fetoprotein (AFP) ≥400 ng / mL và đã được điều trị bằng sorafenib trước đó.
Chỉ định này được FDA phê duyệt vào tháng 5 năm 2019.
CƠ CHẾ TÁC DỤNG
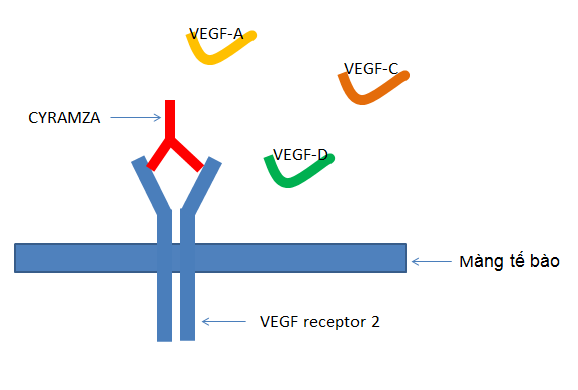
Cyramza liên kết vào ligand của VEGFR 2 để ngăn sự gắn kết VEGFR 2 với VEGF-A, VEGF-C và VEGF-D. Kết quả dẫn đến ức chế sự tăng sinh và hạn chế sự di chuyển các tế bào nội mô của con người.
HIỆU QUẢ LÂM SÀNG
Cyramza được FDA phê duyệt dựa trên kết quả nghiên cứu REACH-2, là một nghiên cứu ngẫu nhiên đánh giá Cyramza so với giả dược ở những bệnh nhân bị ung thư biểu mô tế bào gan đã được điều trị bằng sorafenib trượ́c đó và AFP-High (AFP ≥400 ng / mL). Kết quả cho thấy điều trị bằng Cyramza cải thiện đáng kể thời gian sống sót (OS) của bệnh nhân so với giả dược. Thời gian sống sót trung bình là 8,5 tháng với nhóm Cyramza so với 7,3 tháng với nhóm giả dược. Thời gian sống sót an định không hoá ác (PFS) trung bình là 2,8 tháng với nhóm Cyramza so với 1,6 tháng với nhóm giả dược. Tỷ lệ đáp ứng khách quan cao hơn với Cyramza (4,6%) so với giả dược (1,1%). Ngoài ra, kiểm soát bệnh cao hơn với Cyramza (59,9%) so với giả dược (38,9%).
ĐIỀU TRỊ VỚI CYRAMZA VÀ TÁC DỤNG THƯỜNG GẶP
(Xem thêm tài liệu hướng dẫn sử dụng)
Cyramza được cung cấp dưới dạng dịch tiêm, liều khuyến cáo là 8mg / kg mỗi 2 tuần, truyền tĩnh mạch trong hơn 60 phút. Điều trị tiếp tục cho đến khi bệnh tiến triển hoặc không thể điều trị tiếp do độc tính của thuốc.
Các tác dụng phụ liên quan đến việc sử dụng Cyramza có thể bao gồm: mệt mỏi, phù ngoại biên, tăng huyết áp, đau bụng, giảm sự thèm ăn, tiểu đạm, buồn nôn, cổ trướng, giảm tiểu cầu, hạ đường máu và hạ natri máu.
Nguồn tham khảo:
- https://investor.lilly.com/news-releases/news-release-details/lillys-cyramzar-ramucirumab-becomes-first-fda-approved-biomarker
- https://www.accessdata.fda.gov/drugsatfda_docs/label/2020/125477s034lbl.pdf

Bài viết liên quan
Ung thư Tiêu hóa gan mật
Liệu pháp kết hợp mới trong điều trị ung thư gan được FDA phê duyệt
Di truyền Huyết học
Oxbryta – Thuốc mới điều trị bệnh hồng cầu hình liềm
Da liễu Ung thư
Libtayo – Thuốc mới điều trị ung thư da